导图社区 氧化还原反应
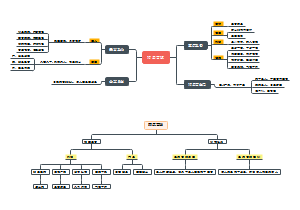
氧化还原反应
氧化还原反应 (oxidation-reduction reaction)是化学反应前后,元素的氧化数有变化的一类反应。 氧化还原反应的实质是电子的得失或共用电子对的偏移。 氧化还原反应是化学反应中的三大基本反应之一(另外两个为(路易斯)酸碱反应与自由基反应) 。自然界中的燃烧,呼吸作用,光合作用,生产生活中的化学电池,金属冶炼,火箭发射等等都与氧化还原反应息息相关。研究氧化还原反应,对人类的进步具有极其重要的意义。
编辑于2022-11-25 09:24:37- 氧化还原反应
- 相似推荐
- 大纲