导图社区 英语名词
- 1.1k
- 78
- 14
- 举报
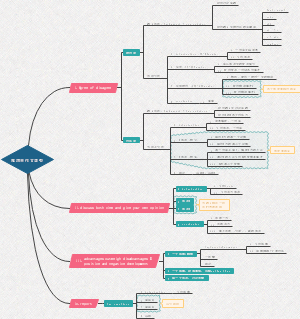
英语名词
在英语语法学习中,学好名词是非常重要的一步,不少同学分不清楚名词的分类,帮你们制作了这张名词思维导图,学起来吧。
编辑于2020-08-09 14:24:29- 相似推荐
- 大纲
名词
定义: 用来表示人,事物,地点以及抽象事物的名称的。
名词的分类
专有名词
人名及头衔:the Queen of England,Winston Churchill
著作名称War and Peace
月份
农历表达the second lunar month /the second month of the lunar calendar
星期
Sunday
节日
Christmas,Mother’s Day
地理名称
国家及大洲
America ,Africa
地区,城市的名称
Rome Beijing
江河湖泊
the Atlantic, the Nile
山脉沙漠等
the Himalayas,the Alps,the Sahara
普通名词:是否可以被分割,形式为意义服务。
名词的数
不可数名词
无法分割的名词,物质。air coffee pork
气体air fog oxygen smoke
液体beer blood coffee ice cream gasoline
固体bread butter cheese meat
组成部份太小而不易数的名词corn sand grass rice snow hair salt sugar
表示总称,通常不可数
总称下的具体概念可数
抽象名词
Advice fun life patience art
这些名词的不同意思可以转化为可数
如学科类math grammar
可数与不可数的相对论
规律一:对于物质名词或总称的名词,若是表示不同的种类,或者因为特定的意思,或者是液体表示“几杯”“几瓶”这样的数量,则转化为可数名词
Food表示不同种类可数
Avoid eating foods that are high in simple carbohydrates,that are,sugar.
Cake表示一块蛋糕
My mother is making a cake .
Milk表不同种类的奶制品
Yogurt contains a higher percentage of Lactic acid than other fermented milk.
Paper表论文报纸
肉类
lamb lambs
glass玻璃不可玻璃杯可数 眼镜只有复数
waters海域只有可数复
因为特定意思转化为可数
Two beers and three coffees表示几瓶几杯
对于抽象名词处于抽象名词若是具体化了则化为可数名词。
Art艺术,an art一门特定的艺术
beauty美丽,a beauty一个美人
Youth青春,a youth一个年轻人
更广泛的说,当一个名词表示抽象的,总称的概念,一般不可数。表示具体的,特定的,一般可数。即,概念不可数,具体事物可数。
Area表面积,不可数如果是指某个地方的具体面积,可数。
The square covers am area of 20,000 square meters.可
Chongqing is the largest city in area in China.不可数。
不能按中文意思的思维理解的可数与不可数。
Money furniture不可数抽象概念
不可数名词的分割
Piece抽象物质
A piece of news
Bottle ,cup drop,glass液态
其他loaf,tube,slice
可数名词
单数
不可数,专有。谓语动词用三单
只用作复数
工具和仪器
Glasses,scissors
服装
Scissors
单形复义
People人民,为person的复数形式
如果是民族,部落,则为普通名词,有单复数变化
The Chinese are an industrious people.
cattle牛群复数
police警察部门警方复数
警官为单数,policeman,policeofficer
poultry家禽,活的,复数
死的肉,单数
规则的复数
+s
S,x,ch,sh,+es
辅音字母+y
变y改I➕es
以o结尾
有生命的es
Tomato hero negro veto(否决)
少数s es 均可
volcano,motto(座右铭)
f,fe结尾
12个变Ves
Calf,knife,life,self,wife,half,leaf,loaf,sheaf(一条一捆),thief,wolf
其余s
少数均可
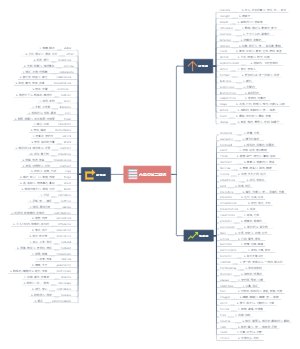
名词的格
名词的格1 ‘s
‘s的所有格 有生命
单数名词+‘s
以s结尾也➕s actress’s
复数名词
直接➕s
children‘s day
以s结尾的直接加’ friends’
复合名词在在最后一个名词前➕s
My father-in-law’s company
并列名词由and连接
共有➕一个’s
各自的在每个名词后➕s
‘S所有格的逻辑关系
所属关系
一个人的
My sister’s boyfriend
一类人的e
Student’s book
主谓关系
Bhutto’s death(die)
British decision =British decide
动宾关系
Bhutto’s assassination (assassinate)
The boy’s punishment= someone punish the boy
同位关系
Bhutto’s loss
表示时间与距离
Today’s newspaper. Fifteen minutes ride
重量或价值等度量
Two pounds’ weight
Ten dollars ‘ worth
国家城市国际组织或地理名词
China’s population Shanghai’s tallest tower the European Union’s export the earth’s surface
交通工具及部件的关系
The plane’s engine
名词所有格修饰的名词被省去
1 避免名词重复
The bike is mine, not Mike’s.
2 店铺或教堂
At the baker’s. At the dentist’s
3 某人的住宅
Go to my sister’s
名词的格2 of属格的构成及逻辑语义关系
1 属格的构成
1 表示无生命的名词所有关系N1+of+N2
the leg of the table
2 当有生命的名词后面接短语动词或从句修饰时
What is the name of the boy sitting next to her?
2 属格的逻辑关系
1 主谓关系,从右往左翻译
The arrival of my mother=my mother arrives
2 动宾关系从左往右翻译
The discussion of the plan
Discuss the plan
3 同位关系
The city of Rome =Rome is a city