导图社区 刑事诉讼流程脑图
- 515
- 59
- 10
- 举报
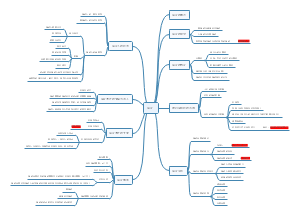
刑事诉讼流程脑图
刑事诉讼是指人民法院、人民检察院和公安机关在当事人及其他诉讼参与人的参加下,依照法律规定的程序,解决被追诉者刑事责任问题的活动,超详细刑事诉讼法流程欢迎大家来看!
编辑于2021-09-05 21:28:43- 刑事诉讼
- 相似推荐
- 大纲
刑事诉讼流程
立案
立案主体
公安机关
检察院
法院
自诉案件的立案,需要满足公诉案件的两个条件和《解释》第259条
1.自行发现;2.单位或个人的报案和举报;3.被害人自行报案;4.犯罪人的自首
立案程序
决定立案
公诉案件:立案决定书
自诉案件:法院自收到自诉书、口头告诉后第2日起15日内作出立案决定
决定不立案
不予立案决定书
控告人不服:1.公安机关:7日以内申请复议,7日内作出复议;2.检察院:10内申请复议,15日内作出复议;3.人民法院:自诉案件15日内作出不立案决定
撤案
撤销案件报告书
立案监督
管辖 P87
立案管辖
人民法院直接受理的刑事案件:自诉案件(1)告诉才处理;(2)被害人有证据证明的轻微刑事案件;(3)被害人有证据证明对被告人对被告人侵犯自己人身、财产权利的行为应当依法追究刑事责任。而公安机关或检察院不予追究被告人刑事责任
公安机关:刑事案件由公安机关受理,除:(1)法院直接受理的案件;(2)军人违反职责的犯罪和军队内部发生的刑事案件;(3)罪犯在监狱内犯罪的刑事案件;(4)其他机关应当管理的
检察院:(1)诉讼活动中行驶法律监督中发现的司法工作人员利用职权实施的非法拘禁、刑讯逼供、非法搜查等侵犯公民权利,损害司法工作的案件;(2)公安机关管辖的国家机关工作人员利用职权实施的重大犯罪案件,需要直接受理时,经省级以上检察院,可以由检察院立案侦查
侦查
侦查主体
公安机关
检察院
侦查行为
讯问犯罪嫌疑人:(1)犯罪嫌疑人对侦查人员的讯问,应当如实回答,有权拒绝回答与本案无关的问题;P61(2)辩护人不能在侦查阶段和犯罪嫌疑人核实证据,律师作为辩护人的,可以在侦查阶段会见犯罪嫌疑人 P122(3)犯罪嫌疑人、被告人供述和辩解P146
询问证人、被害人:(1)只有侦查人员可以询问;P247(2)辩护律师可以经证人或其他有关单位和个人的同意;经检察院、法院许可,被害人或其近亲属、被害人同意,可以向他们收集本案有关材料;P122(3)属于证人证言、被害人陈述的证据类型 P146
勘验、检查:(1)勘验、检查、辨认、侦查实验等笔录之证据 P149
搜查:(1)物证 P141(2)书证 P142
查封、扣押物证、书证
鉴定意见:鉴定意见之证据 P148
通缉:只有公安机关有发布通缉令的权利
特殊侦查措施:(1)技术侦查;(2)秘密侦查
侦查客体:证据及其种类 P141
侦查终结:1.公安机关出具起诉意见书(犯罪情节轻微,依法不需要判处刑罚或免除刑罚的,注明不起诉的条件)检察院决定起诉或不起诉;2.不应对犯罪嫌疑人追究刑事责任案件,应当制作撤销案件决定书,已被逮捕的,应立即释放,发给释放证明,通知原批准的检察院
一般侦查羁押期限:不超过2个月,期限届满不能终结,经上一级人民检察院批准延长1个月(3个月)
重大复杂侦查羁押期限:一般侦查羁押期限届满不能侦查终结,经省、自治区、直辖市检察院批准,可以延长2个月(5个月)
(1)交通不便的边远地区 (2)重大犯罪集团 (3)流窜作案 (4)犯罪涉及面广,取证困难
重刑案件侦查羁押期限:可能判处10年以上有期徒刑,经重大复杂侦查羁押期限不能侦查终结,经省、自治区、直辖市检察院批准或决定,可以延长2个月(7个月)
特殊原因较长时间不宜交付审判的,应当由最高检报请全国人大常委会批准延期审理
侦查期限重新计算:(1)侦查期间发现嫌疑人另有重要罪行(2)嫌疑人不讲真实姓名、住址(身份不明),自查清身份之日起计算
补充侦查:(1)审查起诉阶段的补充审查:可由检察院或公安机关进行审查,一个月内完成,以两次为限;(2)法庭审理阶段的补充侦查:检察机关为主,一个月为限
检察院对直接受理案件的侦查
需要逮捕、拘留由检察院决定、公安机关执行;拘留24小时内讯问
期限:拘留需要逮捕的,14日内作出决定,特殊情况可以延长1-3日
侦查监督
审查起诉
审查起诉
主体:检察院
内容:P274
步骤和方法:审阅案卷材料→讯问→听取被害人意见→听取辩护人意见→进行必要的鉴定活动→调查核实其他证据→补充侦查或补充调查
审查起诉的期限
监察机关、公安机关移送的:应在1个月内作出决定,重大复杂可延长15日
犯罪嫌疑人认罪认罚,符合速裁程序条件,10日作出决定,可能判处1年有期徒刑以上的,可以延长至15日
改变管辖的,从改变后检察院接收案件之日起重新计算
审查起诉的结果
提起公诉 P279:制作起诉书
监察机关采取留置措施,检察院应当对其先行拘留,检察院应在拘留后10日以内作出是否逮捕、取保候审、监视居住,特殊情形可以延长1-4日,决定强制措施的期限不计入审查期限
审查起诉期限:1个月内作出决定,重大复杂可以延长15日;嫌疑人认罪认罚、符合速裁程序适用条件应在10日内作出,可能有期徒刑超过1年的,可以延长至15日
认罪认罚+量刑建议
不起诉 P284:制作不起诉决定书
法定不起诉:(1)没有犯罪事实(2)不认为是犯罪的,危害不大的(3)已过诉讼时效(4)特赦令免除刑罚(5)告诉才处理的,未告诉或撤回告诉的(6)被告人,犯罪嫌疑人死亡的(7)其他法律规定免予追究刑事责任的
酌定不起诉:自由裁量(便宜主义),犯罪情节轻微,依照刑法规定不需要判处刑法或免除刑罚(刑法37)
证据不足不起诉:二次补充侦查的案件,检察院仍然认为证据不足,不符合起诉条件的,应作出不起诉条件;经过一次补充侦查或补充调查,检察院认为证据不足,不符合起诉条件,没有退回补充侦查或补充调查必要的,可以作出不起诉决定
被不起诉书人和涉案财物处理:没收所得及涉案财产的程序
不起诉的限制:(1)公安机关的要求复议、提请复核,监察机关的提请复议(2)被害人的申诉或者起诉(收到不起诉决定书7日内向上一级检察院申诉,向法院起诉)(3)被不起诉人的申诉(收到决定书7日内向检察院申诉)(4)监察机关移送起诉的案件
附条件不起诉 P396:(1)未成年人;(2)罪名属刑法分则第4、5、6章;(3)可能判处1年有期徒刑以下的刑罚;(4)犯罪事实清楚,证据充分,依法应追究刑事责任的起诉条件;(5)必须有悔罪表现;(6)未成年人犯罪嫌疑人及其法定代理人对附条件不起诉无异议
考察时间6个月以上1年以下
撤销附条件不起诉
实施新的犯罪或发现附条件不起诉以前还有其他犯罪需要追诉的
违反治安管理规定或附条件不起诉的监督管理规定,情节严重的
是否需要提起附带民事诉讼:国家、集体财产受到损害,检察院应提起诉讼
强制措施
行使主体:公检法
方式
拘传 P183:未被拘留逮捕的犯罪嫌疑人、被告人依法强制其到案接受讯问
拘传vs传唤:(1)后者无强制力(2)后者适用主体广泛
程序
主体:县级以上公安机关负责人,检察长、法院院长批准,不得少于2人
文件:拘传报告书、拘传证
地点:被拘传人所在地点:(1)工作单位所在市、县(2)户籍地、居住地所在市、县
时间:不得超过12小时,复杂重大的不得超过24小时,从其到案时计算;两次被拘传的间隔不得超过12小时,禁止疲劳审讯
取保候审 P185:提出保证人或者交纳保证金,保证其不妨碍、不逃避诉讼并随传随到
条件:(1)可能判处管制,拘役,独立适用附加刑(2)判处有期徒刑以上刑罚,采取取保候审不致发生社会危险的(3)患有严重疾病,生活不能自理,怀孕或正在哺乳自己婴儿的妇女,采取取保候审不致发生社会危险的(4)羁押期限届满,案件尚未办结,需要采取取保候审的
方式:人保(刑诉69、70),财产保(刑诉72)
被保人的义务:刑诉71:住址、工作单位、联系方式发生变动的,在24小时内向执行机关报告
程序:嫌疑人、被告人及法定代理人、近亲属、辩护人均可申请后,有关机关应在收到书面申请7日内作出是否同意的答复
期限:公检法累计不得超过12个月
监视居住:P190:命令其不得擅自离开住所或居所并对其活动予以监视和控制
一般监视居住(刑诉74)
指定监视居住(刑诉75)
被监视居住人的义务(刑诉77)
程序:(1)由公安机关执行(监视居住决定书,执行监视居住通知书)(2)执行监视居住24小时内通知其家属
期限最长不得超过6个月,但公检法可以在不同阶段连续适用,期间不累计(最长18个月)
指定居所监视居住的期限应折抵刑期,管制,居住1日折抵刑期1日;拘役、有期徒刑的 监视居住2日折抵刑期的1日
拘留:P193:公安机关、检察院遇到法定的紧急情况时,依法临时剥夺某些现行犯或重大嫌疑分子人身自由
期限:一般为3日,特殊情形经县级以上公安机关负责人批准,提请审查批准的时间可以延长1-4日,对于流窜作案、多次作案、结伙作案的重大嫌疑分子,经县级以上公安机关负责人批准时间可以延长至30日;
在30日内不能查清身份的,经县级以上公安机关负责人批准,拘留期限自查清其身份之日起算起;
检察院应当自接到公安机关提请批准逮捕书后的7日内,作出批准逮捕或不批准逮捕的决定;其他机关对直接受理的案件中被拘留的人,认为需要逮捕的,应在14日内作出决定,特殊情况决定逮捕时间可以延长1-3日
对比(1)刑事拘留vs行政拘留(2)刑事拘留vs司法拘留
适用条件:(1)公安机关:刑诉82(2)检察院:刑诉165
拘留程序:拘留证,如果拒绝拘留可以使用戒具,应立即将其送看守所关押,至迟不得超过24小时,在拘留后24小时以内通知其家属,应在24小时内对其进行讯问
逮捕: P196:公检法对起予以羁押,暂时剥夺其人身自由的强制措施
主体:逮捕决定由法院、检察院行使,由公安机关执行
适用条件
文件:(1)公安机关:提请批准逮捕书(2)检察院:批准逮捕决定书、不批准逮捕决定书(3)法院:逮捕决定书(4)逮捕证
期限:(1)检察院:已被拘留的,7日内作出是否逮捕的决定;未被拘留的,应在接到提请i准书后15日内作出是否批准逮捕决定,重大、复杂案件不得超过20日 (2)法院:法院应当将逮捕原因和羁押的处所,在24小时内通知其家属或所在单位,逮捕的被告人,审判人员应在逮捕后24小时内进行讯问 (3)逮捕执行,应立即将其送看守所羁押,应在24小时内通知其家属,逮捕后,应在24小时内讯问 (4)执行逮捕后,应在24内制作逮捕书,送达被逮捕人家属或者单位,但有特殊情形可以不予通知 P201
逮捕后羁押必要性审查 P202
第一审程序
庭前审查 P293:法院对检察院提起公诉的案件进行审查,以决定是否开庭审判的活动
审查内容
审查后的处理:(1)属于告诉才处理的案件,退回检察院,告知受害人有权上诉 (2)不属于本案管辖或被告人不在案的,应当退回检察院 (3)需要补充材料的,通知检察院3日内补送 (4)(依刑诉200.3)宣告被告人无罪后,检察院根据新的事实,证据重新起诉的,依法受理 (5)依《解释》242规定裁定准许撤诉的案件,没有新的事实,证据,重新起诉的,退回检察院 (6)符合刑诉16规定情形的,应裁定终止审理或退回检察院 (7)被告人身份不明,符合刑诉160.2 依法受理
合议庭组成人员(刑诉183)
基层人民法院、中级人民法院审判第一审案件,应当由审判员三人或者由审判员和人民陪审员共三人或者七人组成合议庭进行,
基层人民法院适用简易程序、速裁程序的案件可以由审判员一人独任审判
高级人民法院审判第一审案件,应当由审判员三人至七人或者由审判员和人民陪审员共三人或者七人组成合议庭进行
最高人民法院审判第一审案件,应当由审判员三人至七人组成合议庭进行
人民法院审判上诉和抗诉案件,由审判员三人或者五人组成合议庭进行
庭前准备 P294
开庭前10日前将起诉书副本送达被告人辩护人;通知当事人及其诉讼代理人,法定代理人,辩护人开庭5日前提供证据,证人、鉴定人名单;开庭3日前开庭时间、地点通知检察院;公开审理案件,在开庭3日前公布案由
法庭审判 P295
公诉
开庭:P295
法庭调查:P296
1.公诉人宣读起诉书; 2.被告人、被害人就起诉书指控的犯罪事实分别陈述; 3.讯问、发问被告人,发问被害人(a.公诉人讯问被告人;b.经审判长准许,当事人及其法定代理人、诉讼代理人、辩护人可以向被告人发问;c.经审判长准许,控辩双方可以向被害人、附带民事诉讼原告人发问;d.审判人员讯问被告人,向被害人、附带民事诉讼当事人发问) 4.出示、核实证据(a.询问证人,并非所有证人都要出庭作证;b.询问鉴定人;c.申请有专门知识的人出庭;d.出示、宣读证据;e.调取新证据;f.合议庭调查核实证据)
法庭辩论:P302
公诉人发言→被害人及其诉讼代理人发言→被告人自行辩护→辩护人辩护→控辩双方进行辩论 (检察院可以提出量刑建议并说明理由)
被告人最后陈述
评议和宣判 P304
评议:指控的罪名与审理认定的罪名不一致的,应按照审理认定罪名作出有罪判决
宣判:当庭宣判的,应在5日内送达判决书;定期宣告的,先期公告宣判的时间地点,传唤当事人,通知公诉人,法定代理人,诉讼代理人,判决宣告后,应立即送达判决书
延期审理
中止审理:较长时间无法继续审理的
终止审理(刑诉16)
第一审程序期限:公诉案件应在受理后2个月以内宣判,至迟不得超过3个月; 可能判处死刑的案件或附带民事诉讼的案件,刑诉158情形,经上一级法院批准,可以再延长3个月,特殊情形还需延长的,报请最高院批准 法院改变管辖,从改变后法院收到案件之日起审理期限 检察院补充侦查,补充侦查后移送法院后,法院重新计算审理期限
自诉 P311
不到案的后果:共同被告部分人未告诉,法院应通知其到案,被通知人接到通知后表示不参加诉讼或不出庭的,视为放弃告诉,第一审理结束后,被通知人就同一事实又提起自诉的,法院不受理,但是可以另行提出民事诉讼
自诉人经两次传唤,无正当理由拒不到庭,或未经法庭准许中途退庭,法院按撤诉处理,部分自诉人撤诉或依法裁定撤诉,不影响案件继续审理
附带民事责任部分应依法调节或一并作出判决
可以调节,公诉转自诉例外(刑事调解书);判决宣告前可以自行和解
被告人羁押的,与普通公诉案件第一审的审理期限相同,2个月,最迟不超过3个月 未被羁押的,受理后6个月内
简易程序
时间限制:法院应在受理后20日内审结;可能判处有期徒刑超过3年的,可以延长至1个半月
主体:基础法院
适用条件:案件事实清楚、证据充分;被告人承认自己所犯罪行,对指控的犯罪事实没有异议的;被告人对适用简易程序没有异议的
不适用简易程序的情形:1.被告人是盲聋哑人;2.尚未完全丧失辨认或控制自己行为能力的精神;3.有重大社会影响的;4.共同犯罪中部分被告人不认罪或对适用简易程序有异议的;5.辩护人人作无罪辩护的;6.被告人认罪但经审查可能不构成犯罪的;7.其他情形
人员组成:有期徒刑3年以下,可以组成合议庭或审判员1人独任审判;超过3年的,应当组成合议庭
不受程序限制,但应听取被告人最后陈述意见
速裁程序
时间限制:法院应在受理后10日内审结,对可能判处有期徒刑1年的,可以延长至15日
主体:基层法院
适用条件:法院管辖的可能判处3年有期徒刑以下刑罚的案件;案件事实清楚,证据确实充分;被告人认罪认罚并同意素材程序
不适用的情形:被告人是盲聋哑人;被告人是未成年人;案件有重大社会影响;共同犯罪案件中部分被告人对指控的犯罪事实,罪名,量刑建议或适用速裁程序有异议的;被告人与被害人或其法定代理人没有就附带民事诉讼赔偿等事项达成调解或和解协议;其他不宜适用速裁程序审理的
判决、裁定、决定
判决:法院就案件的实体问题:判决书
不服第一审刑事诉讼的上诉抗诉期限为10日
裁定:法院在审理案件或判决执行过程中对有关诉讼程序和部分实体问题所作的一种处理:裁定书
不服刑事诉讼裁定的上诉,抗诉期限为5日
决定:解决诉讼程序问题一种法院裁判形式:口头或书面
一经作出,立即生效,不得上诉,抗诉(公安检察也可以作出)
第二审程序
两审终审制:一个案件至多经过经过两级法院审判便告终结的审级制度
第二审程序
享有上诉权的当事人及其法定代理人行使上诉权,检察院提起抗诉
第二审法院为作出裁判的第一审法院的上一级法院
第一审法院已经作出判决或裁定,但裁判又尚未发生法律效力的案件
发生法律效力的判决或裁定确有错误,通过审判监督程序
二审是终审程序,所作出的裁判是终审裁判,裁判一经作出,立即发生法律效力
非必经程序
第二审的提起
上诉
提出上诉的主体
当事人:被告人,自诉人,附带民事诉讼原告人,附带民事诉讼被告人
当事人的法定代理人
被告人的辩护人和近亲属
提出上诉的期限
不服第一审刑事诉讼的上诉抗诉期限为10日
不服刑事诉讼裁定的上诉,抗诉期限为5日
接到判决书的第二日起算
上诉方式和途径:上诉人提交上诉状,也可以口头
可以通过原第一审法院,也可以直接向上一级法院提出
上诉的撤回
上诉期内上诉人撤回上诉的,法院应准许,撤回上诉但上诉期间尚未届满,享有上诉权利的人仍可以重新提起上诉
是否上诉,以上诉期内上诉人最后一次表达的意思为准
上诉人在上诉期满后要求撤回上诉的,二审法院应当审查
审查后认为原判事实清楚,适用法律正确,量刑适当,应予准许
审查后认为原判事实不清,适用法律错误,量刑有误,不予准许
被判处死刑立即执行的被告人提起上诉,在二审开庭后裁判宣告前申请撤回上诉的,不予准许
抗诉
抗诉主体
地方各级检察院,抗诉期间,上一级检察院发现下级检察院应当提出抗诉而没有提出抗诉的,可以指令下级检察院依法提出抗诉,但自己不能直接提出抗诉
抗诉的期限
不服第一审刑事诉讼的上诉抗诉期限为10日
不服刑事诉讼裁定的上诉,抗诉期限为5日
接到判决书的第二日起算
提出抗诉的方式和途径
通过原神法院提出抗诉书,并将抗诉书抄送上一级检察院,原审法院应将抗诉书连同案卷证据移送上一级法院,并将抗诉书副本送交当事人
上一级检察院参加公诉
撤回抗诉
在抗诉期间届满前撤回抗诉
上一级检察院对下级检察院提出抗诉的案件,认为抗诉不当的,应当撤回,并通知下级检察院
下级检察院认为上一级检察院撤回抗诉不当的,可以提请复议,上一级检察院应当复议
抗诉可在届满后撤回
第二审的审判
原则
全面审查
案件事实认定,法律适用
上诉抗诉的不服的部分,其他没有异议的部分
实体,程序
共同犯罪未提出上诉抗诉的部分
有利于被害人,不利于被害人
开庭审理
上诉人对一审认定的事实,证据没有异议的案件才可以不开庭审理
上诉不加刑
二审法院对被告人一方提出上诉的案件,经审理后需要撤销原判并作出改判的,改判后不得加重原判刑罚
仅适用被告人或其法定代理人,辩护人,近亲属单方面提出的诉讼
不得以任何理由加重被告人的刑罚
审理方式
开庭审理
被告人,自诉人,法定代理人对第一审认定的事实,证据提出异议,可能影响定罪量刑的案件
被告人判处死刑的上诉案件
检察院提出抗诉的案件
其他
不开庭审理
适用于上诉人仅针对适用法律问题提出异议的案件
二审法院审查认为原判事实不清,证据不足,或具有刑诉238规定的违反法定诉讼程序的情形需要发回重审的,可以不开庭
直接裁判
裁定驳回上诉,抗诉,维持原判
直接改判
发回重审
可以发回重审
原判认定事实不清或证据不足为由发回重审,仅限发回一次
重新审判后对重审后的判决再次提出上诉或检察院提出抗诉,二审法院不得将再次进入二审的案件,再次以原判案件事实不清证据不足为由发回原审法院重审,而应依法作出裁定或判决
应当发回重审
违反回避制度
剥夺或限制当事人的法定诉讼权利,可能影响公正审判
审判组成不合法的
违反公开审判规定
其他
审理期限
受理上诉,抗诉后2个月审结,对可能判处死刑或附带民事诉讼的以及有刑诉158规定情形之一的,可以延长2个月
审判应遵守的刑诉总论部分
刑诉主体
审判机关
检察机关
侦查机关
当事人
犯罪嫌疑人、被告人
被害人
自诉人
附带民事诉讼被告人与原告人
其他诉讼参与人
法定代理人
诉讼代理人
辩护人
辩护与代理 P114
辩护
种类
自行辩护
委托辩护
指定辩护
强制指定辩护
未成年人,盲聋哑人,尚未完全失去辨认和控制能力的精神病人,可能判处无期的,可能判处死刑的
缺席审判
申请指定辩护
因经济困难或其他原因没有委托辩护人,本人和近亲属可以委托
主体
律师
人民团体或嫌疑人被告人所在单位推荐的人
嫌疑人被告人的监护人,亲友
诉讼权利
职务保障
阅卷
会见通信
看守所至迟不超过48小时
调查取证权
提出辩护意见权
获得出庭通知
出庭辩护
拒绝辩护
要求公检法对采取强制措施超过法定期限解除强制措施的权利
侵犯当事人人身权利财产权利违法办案行为依法提出申诉控告
保密
诉讼义务
及时告知办理案件的机关
不在犯罪现场,未达刑事责任年龄,属于不负刑事责任的精神病人,及时告知公检
辩护
不得干扰司法机关诉讼活动
遵守诉讼纪律
不得私受委托,费用,财物
不得违规会见法官,检察官
不得向司法工作人员送礼行贿,或指使当事人行贿
代理
公诉代理
自诉代理
有一定独立地位
证人
翻译人员
回避
回避的适用
回避的理由
回避的程序:提出、审查、决定
管辖
审判管辖
并案管辖
证据与证明
证据:可以用于证明案件事实的材料,但必须经过查证属实,才能作为定案根据
物证:外部特征,存在状态,物质属性
通常为间接证据,不能独立全面的反映案件事实
犯罪工具
犯罪行为侵犯的对象
犯罪现场遗留下的物品或痕迹
犯罪行为产生的物品
书证:文字,符号,图画所表达的思想内容证明案件事实
出生证,身份证护照,工作证,营业执照,账册,账单,票据,合同,书信,日记
直接证据(嫌疑人的书信,日记)
勘验,检查,辨认,侦查实验等笔录
视听资料,电子数据
实物证据
证人证言
被害人陈述
犯罪嫌疑人被告人供述和辩解
供述:承认自己所犯罪行或犯罪事实的陈述
辩解:否认自己实施犯罪行为或犯罪事实的陈述
攀供:揭发同案共犯犯罪事实的陈述,(揭发共同犯罪人另外实施的其他犯罪行为,不属于口供,为证人证言)
鉴定意见
言词证据
原始证据:直接来源于案件事实且未经复制或转述
间接证据:从原始出处以外的来源获取的证据
直接证据:独立,直接证明案件主要事实的证据,不必经过推理过程即可证明案件主要事实
证人证言
被害人陈述
犯罪嫌疑人被告人供述和辩解
书证:文字,符号,图画所表达的思想内容证明案件事实
视听资料,电子数据
间接证据:不能独立,直接证明案件主要事实的证据,需要通过推理并与其他证据结合起来才能证明案件主要事实的证据(证据链)
刑事诉讼法基本原则
侦查权、检察权、审判权由专门机关依法行使原则
法院、检察院依法独立行使审判权、检察权原则
以事实为根据,以法律为准绳原则
依靠群众原则
分工负责、互相制约、互相配合原则
检察院依法对刑事诉讼实行法律监督原则
审判公开原则
有权获得辩护原则
未经法院审判对任何人都不得确定有罪原则
认罪认罚从宽原则
特殊程序
死刑复核程序
中级法院判处死刑的第一审案件,被告人不上诉的,应由高院复核后,报请法院核准,高院不同意死刑的,可以提审或发回重审,高院判处死刑的第一审案件被告人不上诉的,和判处死刑的第二审案件,都应由最高院核准
中级法院判处死刑的第一审案件,被告人不上诉,检察院不抗诉,在上诉,抗诉期满后10日内报请最高院复核
中级法院判处死刑的第一审案件,被告人上诉或检察院抗诉,高院维持死刑判决的,应在作出裁定10日内报请最高院核准
高院判处死刑第一审案件,被告人不上诉,检察院不抗诉,在上诉,抗诉期满后10日内报请最高院核准
依法由最高院核准的死刑案件,判处死缓,在死缓执行期间,如果故意犯罪,查证属实,应执行死刑的,由高院报请最高院核准
死缓核准权归属高级人民法院
中级法院需要报请高级法院核准
高级法院判处死缓的一审案件,被告人不上诉,检察院不抗诉,即作出核准死缓执行的裁定
程序和处理
人员:审判员3人组成合议庭进行
程序
提审被告人→审查核实案卷材料→听取辩护律师意见→认真对待检察院建议→制作复核审理报告
处理
不予核准
核准
审限:未规定期限
审判监督程序(又称再审程序)
法院,检察院对已经发生法律效力的判决和裁定,发现认定事实或适用法律确有错误,依法提起或决定重新审判,以及进行重新审判所应遵循的特别程序
材料来源
当事人及其法定代理人,近亲属的申诉
申诉不能直接引发审判监督程序,不能停止生效裁判的执行
申诉理由刑诉253
向法院提出申诉:由终审法院审查处理,交给上级法院的,通知申诉人向终审申诉,疑难复杂重大,上级法院可直接管辖
向检察院提出申诉:首先由控告申诉部门,监所检察部门分别受理,进行审查,并将结果告知申诉人
公安司法机关自行发现错误裁判
主体
各级法院院长和审判委员会(对本院)
最高院和上级法院(对各级/下级法院)
最高检:对各级法院已发生法律效力的裁判
上级检察院对法院已发生效力的裁判(提请抗诉报告书)
法院应在收到抗诉书后1个月立案
重新审判:一审按一审,二审按二审是最终裁判
一审程序,检察院应通过一审法院向上级法院提出抗诉
二审程序,上一级检察院向同级法院提出抗诉
审理期限:3个月,延长期限不超过6个月,指令下级法院再审,自收到抗诉之日起1个月内做决定
未成年人诉讼程序
当事人和解诉讼程序
缺席审判程序
违法所得的没收程序
执行
最高院执行死刑命令,高级法院交付一审法院执行,一审法院7日内执行,执行3日前,通知同级检察院派员监督
死缓,无期,有期的,公安机关应自收到执行通知书起1个月内将其送交监狱或其他机关执行
有期徒刑在执行刑罚前,剩余刑期在3个月以下的,由看守所代为执行
拘役,公安机关收到执行通知书立即交付执行
未成年人:未成年犯管教所
剥夺政治权利由公安机关执行
管制,宣告缓刑,假释,暂予监外执行的罪犯,社区矫正