导图社区 5、筹资管理 下
- 30
- 0
- 0
- 举报
5、筹资管理 下
财务管理中级职称导图,内容有资金需要量预测、资本成本、杠杆效应、资本结构,希望这份脑图会对你有所帮助。
编辑于2023-09-11 09:11:30 上海- 中级
- 相似推荐
- 大纲
筹资管理(下)
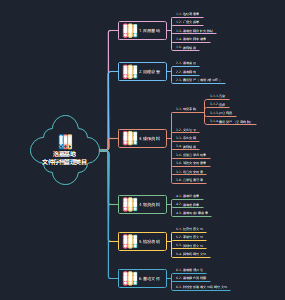
一、 资金需要量预测
1. 因素分析法
1. 含义 又称分析调整法,是以有关项目基期年度的平均资金需要量为基础,根据预测年度的生产经营任务和资金周转加速的要求,进行分析调整,来预测资金需要量的一种方法 计算公式 资金需要量=(基期资金平均占用额-不合理资金占用额)×(1+预测期销售增长率)÷(1+预测期资金周转速度增长率) 特点 计算简便,容易掌握,但预测结果不太精确 适用范围 用于品种繁多、规格复杂、资金用量较小的项目
2. 销售百分比法
2.1. 假设前提
2.1.1. 某些资产、某些负债与营业收入之间存在稳定百分比关系
2.2. 外部融资需求量的计算
1.
2.3. 股利支付率=股利/净利润 利润留存率=1-股利支付率
3. 资金习性预测法
3.1. 按资金习性对资金的分类
3.2. 总资金直线方程
3.2.1. 总资金=不变资金总额+变动资金总额 Y=a+bX
3.3. 估计参数a和b的方法
3.3.1. 回归直线分析法
3.3.2. 高低点法
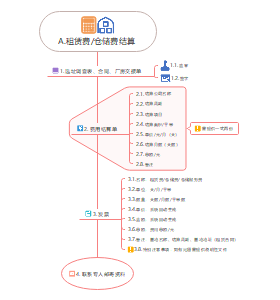
二、 资本成本
1. 资本成本的含义与作用
1.1. 含义:资本成本是指企业为筹集和使用资本而付出的代价,包括筹资费用和占用费用
1.2. 资本成本的作用
1.2.1. 1.资本成本是比较筹资方式、选择筹资方案的依据; 2.平均资本成本是衡量资本结构是否合理的重要依据; 3.资本成本是评价投资项目可行性的主要标准; 4.资本成本是评价企业整体业绩的重要依据。
2. 影响资本成本的因素
3. 个别资本成本的计算
3.1. 资本成本率
3.1.1. =年资金占用费/(筹资总额−筹资费用) =年资金占用费/[筹资总额×(1−筹资费用率)]
3.2. 债券及借款的资本成本计算
3.2.1. 一般模式
3.2.1.1. 债务资本成本率=[年利息×(1−所得税税率)]/[筹资额×(1−筹资费率)]
3.2.2. 贴现模式
3.3. 股权资本成本的计算
3.3.1. 优先股资本成本
3.3.1.1. Ks=D/Pn(1−f)
3.3.1.1.1. 面值*年股息/发行价*(1-筹资费用率)
3.3.2. 普通股资本成本
3.3.2.1. 股利增长模型
3.3.2.1.1. Ks=D0(1+g)/[P0(1−f)]+g D0:当前的股利,本年的股利; D1:预计第一期的股利,期望的股利
3.3.2.2. 资本资产定价模型法
3.3.2.2.1. Ks=Rf+β(Rm-Rf)=国债利率+普通股系数*(市场平均收益率-国债利率)
3.3.2.3. 留存收益资本成本
个别资本成本从低到高的排序: 长期借款<债券<租赁<优先股<留存收益<普通股。
4. 平均资本成本的计算
4.1. 账面价值权数 优点:资料容易取得,且计算结果比较稳定 缺点:不能反映目前从资本市场上筹集资本的现时机会成本,不适合评价现时的资本结构 市场价值权数 优点:能够反映现时的资本成本水平 缺点:现行市价处于经常变动之中,不容易取得;而且现行市价反映的只是现时的资本结构,不适用未来的筹资决策 目标价值权数 优点:能体现期望的资本结构,据此计算的加权平均资本成本更适用于企业筹措新资金 缺点:很难客观合理地确定目标价值
5. 边际资本成本的计算
6. 项目资本成本
6.1. 含义
6.1.1. 是指项目本身所需投资资本的机会成本,即将资本用于本项目投资所放弃的其他投资机会的收益。也可称为项目最低可接受的报酬率
6.2. 使用企业当前综合资本成本作为投资项目资本成本
6.2.1. 1.项目的风险与企业现有资产的经营风险相同; 2.公司继续采用相同的资本结构为项目筹资。
6.3. 运用可比公司法估计投资项目资本成本
6.3.1. 可比公司法
6.3.1.1. 适用范围 如果新项目的经营风险与现有资产的平均经营风险显著不同(不满足等风险假设) 调整方法 寻找一个经营业务与待评价项目类似的上市公司,以该上市公司的β值作为待评价项目的β值 计算步骤 ①卸载可比企业财务杠杆: β资产=可比上市公司的β权益/[1+(1-T可比)×可比上市公司的负债/权益] ②加载目标企业财务杠杆 目标公司的β权益=β资产×[1+(1-T目标)×目标公司的负债/权益] ③根据得出的投资项目β权益计算股东权益成本 股东权益成本=无风险利率+β权益×市场风险溢价 ④计算目标企业的加权平均资本成本 加权平均资本成本=负债税前成本×(1-所得税税率)×负债比重+股东权益成本×权益比重
7. 金融工具价值评估
7.1. 债券价值评估
7.1.1. 债券的基本要素
7.1.1.1. 基本要素 提示 (1)债券面值 到期还本额 (2)票面利率 利息=面值×票面利率 (3)付息方式 付息时点 (4)计息方式 复利计息还是单利计息 (5)债券到期日 持有期限
7.1.2. 债券价值的含义
7.1.3. 债券价值的计算
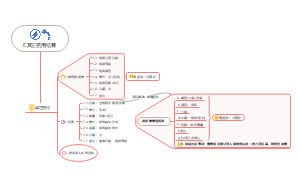
三、 杠杆效应
1. 经营风险与财务风险
2. 杠杆效应
2.1. 含义
2.1.1. 边际贡献(M)=营业收入-变动成本 息税前利润(EBIT)=营业收入-变动成本-固定经营成本 关系公式:EBIT=M-F 税前利润=EBIT-I 净利润=(EBIT-I)×(1-T) 归属于普通股的收益 =净利润-优先股股利 =(EBIT-I)×(1-T)-DP
2.2. 杠杆效应与风险
2.2.1. 经营杠杆效应
2.2.1.1. 是指由于固定性经营成本的存在,而使得企业的资产收益(息税前利润)变动率大于业务量变动率的现象
2.2.1.2. EBIT=销售收入-变动成本-固定性经营成本
2.2.1.3. DOL=(△EBIT/EBIT0)/(△Q/Q0)=息税前利润变动率/产销业务量变动率
2.2.1.4. 存在前提 只要企业存在固定性经营成本,就存在经营杠杆效应 经营杠杆与经营风险 经营杠杆放大了市场和生产等因素变化对利润波动的影响 经营杠杆系数越高,表明资产收益等利润波动程度越大,经营风险也就越大 影响经营杠杆的因素 固定成本比重越高、单位变动成本水平越高、产品销售数量和销售价格水平越低,经营杠杆效应越大,反之亦然
2.2.2. 财务杠杆效应
2.2.2.1. 财务杠杆效应是指由于固定性资本成本(利息、优先股股利等)的存在,而使得企业的普通股收益(或每股收益)变动率大于息税前利润变动率的现象
2.2.2.2. 每股收益(Earnings Per Share)=(净利润−优先股股利)/普通股股数 EPS=[(EBIT−I)×(1−T)−DP]/N
2.2.2.3. 财务杠杆效应的度量指标--财务杠杆系数(Degree Of Financial Leverage) 定义公式: DFL=(△EPS/EPS0)/(△EBIT/EBIT0)=普通股收益变动率/息税前利润变动率 财务杠杆系数=息税前利润/[息税前利润-利息-优先股股息/(1-所得税税率)]
2.2.3. 总杠杆效应
2.2.3.1. 总杠杆效应是指由于固定经营成本和固定资本成本的存在,导致普通股每股收益变动率大于产销业务量变动率的现象
2.2.3.2. 总杠杆系数=经营杠杆系数×财务杠杆系数
2.2.3.3. 意义 ①只要企业同时存在固定性经营成本和固定性资本成本,就存在总杠杆效应 ②总杠杆系数能够说明产销业务量变动对普通股收益的影响,据以预测未来的每股收益水平 ③揭示了财务管理的风险管理策略,即要保持一定的风险状况水平,需要维持一定的总杠杆系数,经营杠杆和财务杠杆可以有不同的组合 影响因素 凡是影响经营杠杆和财务杠杆的因素都会影响总杠杆系数
四、 资本结构
1. 资本结构理论
1.1. 资本结构的含义
1.1.1. 广义的资本结构:包括全部债务与股东权益的构成比例。 狭义的资本结构:指长期负债与股东权益的构成比例
1.2. 最佳资本结构
1.2.1. 是指在一定条件下使企业平均资本成本率最低、企业价值最大的资本结构
1.3. 资本结构理论
1.3.1. MM理论
1.
1.3.2. 其他理论
1. (1)股权代理成本的降低:债务筹资有很强的激励作用,并将债务视为一种担保机制。这种机制能够促使经理多努力工作,少个人享受,并且做出更好的投资决策,从而降低由于两权分离而产生的代理成本(股权代理成本); (2)债务代理成本的增加:债务筹资可能带来另一种代理成本,即企业接受债权人监督而产生的成本
2.
无税的MM理论:V有债=V无债 有税的MM理论:V有债=V无债+PV(利息抵税) 权衡理论:V有债=V无债+PV(利息抵税)-PV(财务困境成本) 代理理论:V有债=V无债+PV(降低股权代理成本)-PV(增加债务代理成本) 优序融资理论:先内后外,先债后股。
2. 影响资本结构的因素
2.1. 1.企业经营状况的 稳定性和成长率 如果产销业务稳定,并能够以较高的水平增长,企业可以采用高负债的资本结构 2.企业的财务状况 和信用等级 企业财务状况良好,信用等级高,企业容易获得债务资本 3.企业资产结构 拥有大量固定资产的企业主要通过发行股票融通资金;拥有较多流动资产的企业更多地依赖流动负债融通资金 资产适用于抵押贷款的企业负债较多;以技术研发为主的企业则负债较少 4.企业投资人和 管理当局的态度 如果股东重视控制权问题,企业一般尽量避免普通股筹资;稳健的管理当局偏好于选择低负债比例的资本结构 5.行业特征和 企业发展周期 产品市场稳定的成熟产业经营风险低,因此可提高债务资本比重,发挥财务杠杆作用 高新技术企业产品、技术、市场尚不成熟,经营风险高,因此可降低债务资本比重,控制财务风险 企业初创阶段,经营风险高,在资本结构安排上应控制负债比例;企业发展成熟阶段,产品产销业务量稳定和持续增长,经营风险低,可适度增加债务资本比重,发挥财务杠杆效应;收缩阶段,产品市场占有率下降,经营风险逐步加大,应逐步降低债务资本比重 6.经济环境的税务 政策和货币政策 当所得税税率较高时,债务资本的抵税作用大,企业充分利用这种作用以提高企业价值;当国家执行了紧缩的货币政策时,市场利率较高,企业债务资本成本增大
3. 资本结构优化
3.1. 每股收益分析法