导图社区 模块IV
- 44
- 0
- 0
- 举报
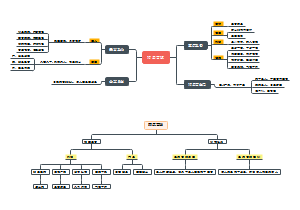
模块IV
基本原理 I-V转换最简单的方式就是串一个电阻,如图a,一般大电流的时候使用采样电阻R即可实现IV转换,再加上运放放大或者射随就可以ADC模块直接采集,在这里我们介绍的是微弱电流的IV...
编辑于2022-11-21 19:22:20- 相似推荐
- 大纲
模块IV
注意事项
考马斯亮蓝测定蛋白质含量中需要注意哪些事项?
答:要在试剂加入后的5~20min内测定光吸收值,因为这段时间内颜色最稳定。测定完成后可用乙醇将比色皿洗干净。
双缩脲法测定蛋白质含量中需要注意哪些事项?
答:须于显色后30min内测定,且各管由显色到比色的时间应尽可能一致。样品蛋白质含量应在标准曲线范围内。
紫外吸收法测定蛋白质含量中需要注意哪些事项?
多种有机物,如醇、酮、醛、醚、有机酸、酰胺类和过氧化物等都有干扰作用。所以最好用无机盐、无机碱和水溶液进行测定。若含有有机溶剂,可先将样品蒸干,或用其他方法除去干扰物质,然后用水、稀酸和稀碱溶解后再做测定。
实验结果
分光光度
现象
数据
双缩脲
现象
数据
考马斯亮蓝
现象
数据
紫外吸收
数据
操作方法
分光光度法
双缩脲法
考马斯亮蓝法
紫外吸收法
实验试剂
双缩脲实验的试剂
(1)标准酪蛋白溶液 用0.05 mol/L NaOH溶液配制。酪蛋白要预先测定其蛋白质纯度,再根据其纯度配制成标准溶液。也可用牛血清蛋白或卵其清白蛋白配制标准蛋白溶液。 (2)双缩脲试剂:溶解1.5g CusO4·5H2O和6.0gNaKC4H4O6。4H2O于500ml蒸馏水中,在搅拌下加入300ml10% NaOH溶液,用蒸馏水定容到1升刻度,混匀备用。 (3)蛋白质样品或蛋白质样品溶液。
考马斯亮蓝实验的试剂
(1)考马斯亮蓝试剂 考马斯亮蓝G-250 100mg溶于50 ml 95%乙醇中,加入100ml85%磷酸,用蒸馏水稀释至1000ml。 (2)标准蛋白质溶液牛血清蛋白或卵其清白蛋白等,预先测定其蛋白纯度,再根据纯度用蒸馏水或0.9%NaCl 准确配制。
紫外吸收实验的试剂
(1)样品蛋白溶液 准确称样品蛋白质,配制成一定浓度的溶液。
基本原理
分光光度法
分光光度法是利用物质分子对光的选择性吸收进行鉴别物质或测定其含量的技术。因为分光光度法极为灵敏、精确、快速和简便,在复杂组分的系统中,不需要分离,即能检测出其中所含的极少量物质,因此为生物化学研究中广泛使用的方法之一。光波和其他波一样,具有一定的频率(v)。不同单色光的颜色不同,就是因为其频率不同。但不同频率的光在真空中的传播速度(c)相同,都是3×108m/s。根据光的速度(c)和频率(v)可计算出它的波(入)生化研究中用于测定物质含量的光谱范围,通常包括波长范围为400-760nm的可见光区和波长范围为200-400nm的紫外光区。钨灯能发出400-760nm波长的光谱,可作为可见光分光光度计的光源。氢灯能发出185-400nm波长的光谱,可作为紫外分光光度计的光源。如果在光源和棱镜之间放上某种物质的溶液,此时在屏上所显示的光谱已不再是光源的光谱,它出现了几条暗线,即光源发射光谱中某些波长的 光因溶液吸收而消失,这种被溶液吸收后的光谱称为该溶液的吸收光谱。不同物质的吸收光谱是不同的。
双缩脲法定量测定蛋白质含量原理
在碱性溶液中,双缩脲(H,N-CO-NH-CO-NH,)与Cu2+作用形成紫红色的络合物,这一反应称双缩脲反应。具有两个或两个以上肽键的化合物都有双缩脲反应,因此蛋白质在碱性溶液中,也能与Cu2+形成紫红色络合物,颜色深浅与蛋白质浓度成正比,而与蛋白质分子量及氨基酸成分无关,故可用比色法测定蛋白质的浓度。在一定条件下,未知样品的溶液与标准蛋白质溶液同时反应,并于540nm下比色,可以通过标准蛋白质的标准曲线求出未知样品的蛋白质浓度。测定范围为1~10mg蛋白质。
考马斯亮蓝法定量测定蛋白质含量原理
考马斯亮蓝法测定蛋白质浓度,属于染料结合法的一种。考马斯亮蓝G-250 (coomassie brilliant blue, CBB)在游离状态下呈红色,当它与蛋白质结合后变为蓝色,在一定蛋白质浓度范围内,蛋白质.色素结合物在595nm波长下的光吸收符合比尔定律,故可用于蛋白质的定量分析。蛋白质与考马斯亮蓝G-250结合2min左右达到平衡。该反应非常灵敏,可测微克级蛋白质含量。
紫外吸收法定量测定蛋白质含量原理
蛋白质具有吸收紫外线的性质,吸收高峰在280nm波长处。在此波长范围内,蛋白质溶液的光吸收值(O.Dzeo)与其含量呈正比关系,可用作定量测定。将待测蛋白质溶液适当稀释,在波长260nm和280nm处分别测出O.D值,然后利用280nm及260nm下的吸收差求出蛋白质的浓度。计算:蛋白质浓度(mg/ml)=1.45O.D280—0.74O.D260。
实验器材
双缩脲实验的器材
(1)容量瓶(2)试管、试管架(3)恒温水浴槽(4)吸量管(5)分光光度计(6)电热套(7)锥形瓶(8)比色皿
考马斯亮蓝实验的器材
(1)容量瓶(2)试管及试管架(3)恒温水浴槽4)吸量管(5)分光光度计(6)电热套
紫外吸收实验的器材
(1)紫外分光光度计(2)容量瓶(3)试管、试管架(4)吸量管(5)锥形瓶(6)比色皿
思考题
你对分光光度法中“空白设置”的认识
1.试样空白
显色剂没有颜色而试液有颜色,或者说在测量波长处,显色剂无吸收,试液有吸收时,应采用不加显色剂的试液作参比溶液,称为试样空白。
2.溶剂空白
当试液、显色剂及所作用的其他试剂在测定波长处都无吸收时,可采用纯溶剂(如蒸馏水)做参比溶液,称为溶剂空白。
3.试剂空白
若显色剂有颜色,并且在测量波长处有吸收,但试液在测量条件下没有吸收,在这种情况下,可用不含试液而显色剂和其他试剂都相同的溶液作参比溶液,称为试剂空白。
4.褪色空白
能够多选择性地与有色络合物中的被测离子作用,使络合物破坏而褪色,然后以它作为参比溶液的一种试剂,称为褪色空白。
以考马斯亮蓝法测定某蛋白质粉末样品为案例,请述“生物学重复”的设置及意义
通过相同背景和处理的生物学重复,可以实现消除组内的误差,提高检验的灵敏度,还可以通过比较生物学重复来测量样本间的差异程度,以此来挖掘在组内具有普遍规律性的结论。
结合结果的比较与分析综合探讨三种测定方法的异同点(各自的优缺点及应用特点)
双缩脲法的优点是:操作简单,显色稳定,重复性好。 双缩脲法的缺点是:最大的缺点是灵敏度较低,适用于毫克级蛋白质的测定。 Tris、铵盐对测定有干扰,有大量脂肪性物质同时存在时,会产生混浊的反应混物。 考马斯亮蓝染色法的优点:灵敏度高(比Lowry法灵敏4倍),测定范围可以是1~1000μg/ml蛋白质,测定快速,简洁。 考马斯亮蓝染色法的缺点:由于各种蛋白质中的精氨酸和芳香族氨基酸的含量不同,因此 Bradford 法用于不同蛋白质时有较大的偏差。显色剂的稳定性较差。 紫外吸收法的优点是:快速、简便、不消耗样品,低浓度盐类NaCl、(NH4),SO,以及0.1mol/L H,PO4、HgBO,、Tris等缓冲液都无明显干扰作用。因此,在蛋白质和酶的生化制备中(特别是在柱层析分离中)广泛应用。 紫外吸收法的缺点是:若样品中含有大量吸收紫外线的物质,会出现较大的干扰。
模块IV
注意事项
考马斯亮蓝测定蛋白质含量中需要注意哪些事项?
答:要在试剂加入后的5~20min内测定光吸收值,因为这段时间内颜色最稳定。测定完成后可用乙醇将比色皿洗干净。
双缩脲法测定蛋白质含量中需要注意哪些事项?
答:须于显色后30min内测定,且各管由显色到比色的时间应尽可能一致。样品蛋白质含量应在标准曲线范围内。
紫外吸收法测定蛋白质含量中需要注意哪些事项?
多种有机物,如醇、酮、醛、醚、有机酸、酰胺类和过氧化物等都有干扰作用。所以最好用无机盐、无机碱和水溶液进行测定。若含有有机溶剂,可先将样品蒸干,或用其他方法除去干扰物质,然后用水、稀酸和稀碱溶解后再做测定。
实验结果
分光光度
现象
数据
双缩脲
现象
数据
考马斯亮蓝
现象
数据
紫外吸收
数据
操作方法
分光光度法
双缩脲法
考马斯亮蓝法
紫外吸收法
实验试剂
双缩脲实验的试剂
(1)标准酪蛋白溶液 用0.05 mol/L NaOH溶液配制。酪蛋白要预先测定其蛋白质纯度,再根据其纯度配制成标准溶液。也可用牛血清蛋白或卵其清白蛋白配制标准蛋白溶液。 (2)双缩脲试剂:溶解1.5g CusO4·5H2O和6.0gNaKC4H4O6。4H2O于500ml蒸馏水中,在搅拌下加入300ml10% NaOH溶液,用蒸馏水定容到1升刻度,混匀备用。 (3)蛋白质样品或蛋白质样品溶液。
考马斯亮蓝实验的试剂
(1)考马斯亮蓝试剂 考马斯亮蓝G-250 100mg溶于50 ml 95%乙醇中,加入100ml85%磷酸,用蒸馏水稀释至1000ml。 (2)标准蛋白质溶液牛血清蛋白或卵其清白蛋白等,预先测定其蛋白纯度,再根据纯度用蒸馏水或0.9%NaCl 准确配制。
紫外吸收实验的试剂
(1)样品蛋白溶液 准确称样品蛋白质,配制成一定浓度的溶液。
基本原理
分光光度法
分光光度法是利用物质分子对光的选择性吸收进行鉴别物质或测定其含量的技术。因为分光光度法极为灵敏、精确、快速和简便,在复杂组分的系统中,不需要分离,即能检测出其中所含的极少量物质,因此为生物化学研究中广泛使用的方法之一。光波和其他波一样,具有一定的频率(v)。不同单色光的颜色不同,就是因为其频率不同。但不同频率的光在真空中的传播速度(c)相同,都是3×108m/s。根据光的速度(c)和频率(v)可计算出它的波(入)生化研究中用于测定物质含量的光谱范围,通常包括波长范围为400-760nm的可见光区和波长范围为200-400nm的紫外光区。钨灯能发出400-760nm波长的光谱,可作为可见光分光光度计的光源。氢灯能发出185-400nm波长的光谱,可作为紫外分光光度计的光源。如果在光源和棱镜之间放上某种物质的溶液,此时在屏上所显示的光谱已不再是光源的光谱,它出现了几条暗线,即光源发射光谱中某些波长的 光因溶液吸收而消失,这种被溶液吸收后的光谱称为该溶液的吸收光谱。不同物质的吸收光谱是不同的。
双缩脲法定量测定蛋白质含量原理
在碱性溶液中,双缩脲(H,N-CO-NH-CO-NH,)与Cu2+作用形成紫红色的络合物,这一反应称双缩脲反应。具有两个或两个以上肽键的化合物都有双缩脲反应,因此蛋白质在碱性溶液中,也能与Cu2+形成紫红色络合物,颜色深浅与蛋白质浓度成正比,而与蛋白质分子量及氨基酸成分无关,故可用比色法测定蛋白质的浓度。在一定条件下,未知样品的溶液与标准蛋白质溶液同时反应,并于540nm下比色,可以通过标准蛋白质的标准曲线求出未知样品的蛋白质浓度。测定范围为1~10mg蛋白质。
考马斯亮蓝法定量测定蛋白质含量原理
考马斯亮蓝法测定蛋白质浓度,属于染料结合法的一种。考马斯亮蓝G-250 (coomassie brilliant blue, CBB)在游离状态下呈红色,当它与蛋白质结合后变为蓝色,在一定蛋白质浓度范围内,蛋白质.色素结合物在595nm波长下的光吸收符合比尔定律,故可用于蛋白质的定量分析。蛋白质与考马斯亮蓝G-250结合2min左右达到平衡。该反应非常灵敏,可测微克级蛋白质含量。
紫外吸收法定量测定蛋白质含量原理
蛋白质具有吸收紫外线的性质,吸收高峰在280nm波长处。在此波长范围内,蛋白质溶液的光吸收值(O.Dzeo)与其含量呈正比关系,可用作定量测定。将待测蛋白质溶液适当稀释,在波长260nm和280nm处分别测出O.D值,然后利用280nm及260nm下的吸收差求出蛋白质的浓度。计算:蛋白质浓度(mg/ml)=1.45O.D280—0.74O.D260。
实验器材
双缩脲实验的器材
(1)容量瓶(2)试管、试管架(3)恒温水浴槽(4)吸量管(5)分光光度计(6)电热套(7)锥形瓶(8)比色皿
考马斯亮蓝实验的器材
(1)容量瓶(2)试管及试管架(3)恒温水浴槽4)吸量管(5)分光光度计(6)电热套
紫外吸收实验的器材
(1)紫外分光光度计(2)容量瓶(3)试管、试管架(4)吸量管(5)锥形瓶(6)比色皿
思考题
你对分光光度法中“空白设置”的认识
1.试样空白
显色剂没有颜色而试液有颜色,或者说在测量波长处,显色剂无吸收,试液有吸收时,应采用不加显色剂的试液作参比溶液,称为试样空白。
2.溶剂空白
当试液、显色剂及所作用的其他试剂在测定波长处都无吸收时,可采用纯溶剂(如蒸馏水)做参比溶液,称为溶剂空白。
3.试剂空白
若显色剂有颜色,并且在测量波长处有吸收,但试液在测量条件下没有吸收,在这种情况下,可用不含试液而显色剂和其他试剂都相同的溶液作参比溶液,称为试剂空白。
4.褪色空白
能够多选择性地与有色络合物中的被测离子作用,使络合物破坏而褪色,然后以它作为参比溶液的一种试剂,称为褪色空白。
以考马斯亮蓝法测定某蛋白质粉末样品为案例,请述“生物学重复”的设置及意义
通过相同背景和处理的生物学重复,可以实现消除组内的误差,提高检验的灵敏度,还可以通过比较生物学重复来测量样本间的差异程度,以此来挖掘在组内具有普遍规律性的结论。
结合结果的比较与分析综合探讨三种测定方法的异同点(各自的优缺点及应用特点)
双缩脲法的优点是:操作简单,显色稳定,重复性好。 双缩脲法的缺点是:最大的缺点是灵敏度较低,适用于毫克级蛋白质的测定。 Tris、铵盐对测定有干扰,有大量脂肪性物质同时存在时,会产生混浊的反应混物。 考马斯亮蓝染色法的优点:灵敏度高(比Lowry法灵敏4倍),测定范围可以是1~1000μg/ml蛋白质,测定快速,简洁。 考马斯亮蓝染色法的缺点:由于各种蛋白质中的精氨酸和芳香族氨基酸的含量不同,因此 Bradford 法用于不同蛋白质时有较大的偏差。显色剂的稳定性较差。 紫外吸收法的优点是:快速、简便、不消耗样品,低浓度盐类NaCl、(NH4),SO,以及0.1mol/L H,PO4、HgBO,、Tris等缓冲液都无明显干扰作用。因此,在蛋白质和酶的生化制备中(特别是在柱层析分离中)广泛应用。 紫外吸收法的缺点是:若样品中含有大量吸收紫外线的物质,会出现较大的干扰。