导图社区 二级建造师矿业井巷工程
- 107
- 2
- 1
- 举报
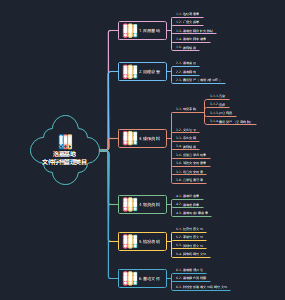
二级建造师矿业井巷工程
二级建造师矿业工程井巷工程思维导图,分享了立井井筒施工、巷道与硐室施工的知识,大家可以学起来哦。
编辑于2023-05-05 15:01:50 山西- 二级建造师
- 井巷工程
- 矿业工程
- 相似推荐
- 大纲
井巷工程
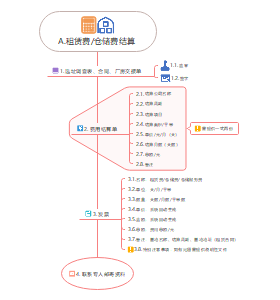
立井井筒施工
表土施工方法及应用
表土分类:稳定(水少)、不稳定(水多)
井筒表土普通施工法(吊板)
井圈背板法(临时支护):特点临时支护段高不大于2m,掘进不超过30m,由下向上拆除井圈、背板,砌筑永久井壁,重复到基岩;适用于较稳定土层
吊挂井壁法:短段掘砌特点施工段高0.5-1.5m,接槎多封水性能差,配置超前小井降低水位,复砌第二场井壁;适用流动小,水压小的土层
板桩施工法:木桩3-6m土层,金属桩8-10m土层,不稳定土层
特殊施工法
冻结法:冻结孔钻进、地层冻结、井筒掘砌、冻结管拔除、冻结空充填;一次冻全深、局部冻结、差异冻结和分期冻结(由上而下),深入稳定层10m及以上;含水、淤泥、饱和地层
钻井法:井筒钻进、泥浆护壁洗井排渣、下沉预制井壁(注水下沉)和壁后注浆固井;钻压(钻头重量,正常:70%;过渡:50%);洗井(井径大于等于3m反循环洗井(吸管喝奶茶方式,效率高));深入稳定层5m及以上
沉井法(超前支护):需刃脚,涌水大,表土厚使用淹水沉井(不抽水开挖);不含卵石、漂石,总厚度100m左右的表土层
注浆法:包括地面(小于1000m)、工作面(段高30-50m)、壁后(整体工段从上往下逐段注浆;段内由下往上注浆,再由上往下复注一次);地面(含水层多,间距小);工作面(含水层深,间距大);深入地板10m及以上;适用裂隙、破碎、溶洞
帷幕法:超前支护,深入稳定层3-6m,适用深度小于100m的表土
基岩施工工艺
钻眼爆破法:钻眼爆破工作(循环时间20%-30%)-装岩与提升-井筒支护工作-通风、排水、测量等辅助工作
立井基岩宜采用伞钻钻眼,深度3-5m(井筒直径小于5m——手持式风动凿岩机,深度1.5-2m)
伞钻:支撑臂、推进系统、中央立柱、动臂、凿岩机
爆破器材
抗水炸药,许用水胶炸药、乳化炸药
有瓦斯或煤尘爆炸或井筒穿过煤层进行爆破,必须采用煤矿安全炸药和延时不超过130ms的毫秒延期电雷管
电源采用交流电源或专用起爆器,不得超过380V
爆破参数:直径、深度、数目、炸药消耗量;短段掘砌混合作业3.5-5m,伞钻
爆破图表(参始布效):爆破原始条件、爆破参数表、炮眼布置图及预期爆破效果
装岩提升工作(最费时50%-60%)
装岩工作
中心回转式抓岩机(HZ型):固定在吊盘下层盘或稳绳盘上;利用变幅机构作径向运动,利用回转机构作圆周运动,利用提升机构上下运动抓岩
提升工作
提升容器、钩头联结装置、提升钢丝绳、天轮、提升机以及提升必需的导向稳绳和滑架组成,可设1-3套单钩提升或一套单钩一套双沟提升
排矸工作:提升地面井架上翻矸台,翻矸装置将矸石卸出,溜矸槽或矸石仓卸入汽车或矿车
井筒支护工作:掘进一定的深度后再进行永久支护工作,必须及时进行临时支护
临时支护:短段作业,可不采用临时支护,采用锚喷支护
永久支护:多数井筒采用整体混凝土井壁,配比必须经由有资质单位试验确定,强度现场预留试块进行试压确认
溜灰管或吊桶输送到井下注入模板内,必须制定安全技术措施,强度等级大于C40或输入深度大于400m,严禁采用溜灰管输送(双4,石子砂浆分离)
模板
采用长段掘砌,多采用液压滑升模板或装配式金属模板
采用短段掘砌,多采用金属整体活动模板,稳岩中3-4.5m
立井施工辅助工作
通风工作:最多人数计算时,每人每分钟不应小于4立方米;炮烟排出放炮后15min排出。可采用压入式、抽出式或抽出辅以压入式通风
井筒涌水:注浆堵水、导水与截水、钻孔泄水和井筒排水
压风和供水:压风管和供水管
其他辅助工作:供电、照明、通信与信号的设置、测量以及布置安全梯
施工作业方式及其机械化配套方案
立井井筒施工作业方式
掘、砌单行作业:若干段高,从上而下逐段施工。同一段高内,掘、砌交替顺序施工,当井筒涌水量小于40立方每小时,任何地质条件均可。特别井筒深度小于400m,施工管理技术水平薄弱,凿井设备不足,应首先考虑
长段单行作业:规定段高内,自上而下掘进,同时进行临时支护,掘至设计的井段高度时,由下而上砌筑永久井壁
优点:井筒施工质量,减少混凝土接槎缝
缺点:需要临时支护,增加施工成本和工期
井圈背板临时支护30m-40m,最大不超过60m,支护时间不超过1个月,材料消耗大,安全可靠性也低
锚喷临时支护可采用较大段高
短段掘、砌单行作业
优点:不需要临时支护,降低成本和工期
缺点:接槎缝比较多
掘、砌平行作业:需要临时支护,现很少采用;当井筒基岩深度大于400m,井筒净直径大于6m,围岩稳定,井筒涌水量小于20立方每小时,施工装备技术力量强可用
掘、砌混合作业:部分平行,混合作业是在向模板浇筑混凝土达1m高左右时,继续筑混凝土的同时,可装岩出渣
优点:节省工期
缺点:采用溜灰管输送或两套提升系统,劳动组织相对复杂,一般直径超6.5m的井筒中,在冻结表土段施工常见
掘砌安一次成井:很少使用
立井井筒施工常用机械化配套方案
设计原则
根据工程条件,施工队伍素质和已具有设备条件综合考虑
设备之间能力要匹配:排矸-提升-装岩-爆破-支护-掘进-辅助
短段单行作业或混合作业
降低劳动强度
加大提升能力
作业线配套方案
伞钻:钻眼最大4.5m,井筒直径小于6m,考虑4臂;井筒直径大于8m,考虑9臂
抓岩机:直径大于8m,考虑1.0立方的或两台
提升机:井筒直径6-9用2套,小于6用1套,大于9用3套;有2的为双滚筒,主、风井,一个单滚筒,一个双滚筒
凿井井架:四型(深度800m)、五型(深度大于1000)
凿井绞车:带A的时安全梯专用绞车
模板:液压整体金属活动式模板高度与伞钻钻眼深度匹配(炮眼利用率80%算)
水泵:扬程与井深匹配,注意多级泵(80*6)
井壁结构及其施工技术要求
立井井壁结构
砌筑井壁:很少采用
整体浇筑式井壁:穿过不稳定表土层、断层破碎带等,以及承担井塔荷载的井颈部分使用
锚喷井壁:仅限主井风井中采用
装配式井壁
复合井壁:两层以上井壁组合而成,多用于冻结法凿井的立井井筒,达到防水、高强、两层井壁间可滑动三方面的要求
井壁施工技术要求
锚喷支护的井壁施工
喷浆、喷射混凝土的强度、厚度、锚杆的锚固力应附合设计要求
井筒的内半径应附合设计和允许偏差要求
锚杆的间距、深度、数量及规格应附合设计要求
锚喷支护的外观质量要求:无离层、无剥落、五裂缝、无露筋、锚杆尾端不外露
浇筑式混凝土井壁施工要求
木模板高度不宜超过1.2m,厚度不应小于50mm,宽度不宜大于150mm
装配式钢模板高度不宜超过1.2m,厚度不应小于3.5mm
整体活动式钢模板高度2-5m,厚度满足刚度要求;稳车上或吊盘下,其悬吊点不得少于3个
整体滑升模板高度宜为1.2-1.4m,厚度不应小于3.5m
组装后的模板,外沿半径应大于井筒设计净半径的10-40mm,上下面保持水平,允许误差10mm
应使用商品混凝土
钢筋混凝土井壁宜采用钢筋直螺纹连接,连接强度不应小于整体钢筋强度
井壁混凝土应对称入模,分层浇筑(初凝时间内,厚度宜为0.3-0.4m),滑升间隔时间不得超过1h
输送混凝土底卸式吊桶和溜灰管,使用溜灰管输送混凝土,坍落度不应小于150mm,石子粒径不大于40mm,内径不小于150mm,末端安设缓冲装置采用分灰器入模
脱模时混凝土强度,采用滑升模板,应0.05-0.25MPa;采用整体组合钢模,应0.7-1.0MPa;钢木模板,不得小于1.0MPa
应做好井壁隐蔽工程记录:自检-验收申报-通知监理/甲方检查-试验合格
施工防治水方法及应用
注浆堵水
预注浆
地面预注浆:含水层地表较浅时,采用地面预注浆。含水层比较薄,一次注完全深,含水层厚,分段注浆
厚含水层:一种自上向下分段钻孔,注浆效果好,注浆孔复钻工程量大;另一种注浆孔一次钻到含水层以下3-4m,自下向上借助止浆塞分段注浆,不需复钻,效果不如分段钻孔注浆
地面预注浆结束标准
水泥浆注浆,压力达到终压,继续以同样压力注入较稀浆液20-30min,停止孔段注浆工作
水泥-水玻璃浆液,达到终压保持稳定10min,可结束孔段注浆工作
黏土-水泥浆浆液,终压稳定20-30min后,可结束孔段注浆工作
工作面预注浆:含水层埋藏较深,采用工作面预注浆。井筒掘进到含水岩层一定距离停止掘进,构筑混凝土止水垫,预测井筒涌水量超过10立方米每小时,采取工作面注浆措施
壁后注浆:自上而下分段进行
注浆段壁后为冲积层,注浆孔深度应小于井壁厚度200mm
双层井壁,注浆孔应穿过内层井壁进入外层井壁,外层井壁深度不应大于100mm
注浆孔穿透井壁注浆时,应制度专项安全措施,注浆管后为含水层,注浆孔宜进入岩层1000mm以上
检查涌水量较大或涌水中含砂时,应停止钻进并及时注浆
井筒排水
吊桶排水:涌水量不超过10立方每小时,用风动潜水泵将水排入吊桶或排入装满矸石吊桶的空袭内,提升设备提到地面排出
吊泵排水:涌水量不超过40立方每小时
卧泵排水:吊盘设置水箱和卧泵,工作面涌水用风动潜水泵排入吊盘水箱;优点不占用井筒空间,故障率低,易于维护,流量大扬程大
截水和泄水
表土施工降水
工作面降低水位法:超前小井或超前钻孔
井外疏干降低水位法:井筒周围钻孔,抽水降低水位
施工辅助生产系统及技术要求
提升系统
通风系统
排水系统
压风和供水系统
施工主要设备及其应用
井筒掘进施工设备
钻眼设备
手持式凿岩机
伞形钻架:钻眼深度3-5m,必须设置保险绳
装岩设备:中心回转抓岩机(HZ)
井筒砌壁施工模板:整体现浇混凝土井壁结构
金属拆卸式模板:不好用,不机械化
金属伸缩式活动模板(液压整体金属式活动模板)依靠伸缩缝
整体滑升模板:长段、连续作业
其他施工设备或设施:凿井井架、天轮平台、卸矸台、封口盘、固定盘、吊盘、提升机和凿井绞车
凿井井架:亭式井架6种型号,天轮平台位于凿井井架顶部,保证足够的过卷高度(4m)、伞钻进出高度,可利用永久井架
卸矸台:翻卸矸石的工作平台
封口盘与固定盘
封口盘:也叫井盖,工作平台,又保护井上下作业人员安全的结构物
固定盘:进一步保护作业人员安全,位于封口盘下4-8m,设有井筒测量装置,有时也作为接各种管道的工作台
吊盘与稳绳盘
吊盘:进行井筒永久支护的工作盘和工作面操作工人的保护盘,4根钢丝绳悬挂再地面凿井绞车。短段掘砌单行作业和混合作业中,又可用于拉紧稳绳、安设抓岩机等设备;双层吊盘或三层吊盘,两层盘之间距离4m
稳绳盘:采用掘砌平行作业,井筒内设有砌壁吊盘和稳绳盘。拉紧稳绳、安设抓岩机
提升机与凿井绞车
提升机:用于井筒施工的提升工作
凿井绞车:用于悬吊凿井设备,包括单滚筒,双滚筒,安全梯专用凿井绞车
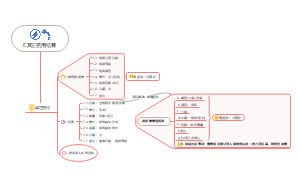
巷道与硐室施工
巷道及硐室的施工程序和施工方法
基本程序:钻眼爆破(综掘切割)、出渣钉道、巷道支护、水沟掘砌、管线安设及通风和安全检查
钻眼爆破法:气腿式凿岩机加耙斗装载机(常规)或凿岩台车加挖斗式装岩机;耙斗装载机配备气动调车盘或胶带转载机,缩短调车时间
钻眼爆破
钻眼工作
气腿式凿岩机:可多台同时作业,可实现钻眼与装岩工作平行作业
凿岩台车:钻眼工作全面机械化,效率高;不能钻眼装岩平行作业,周边眼定位难度较大
钻装机打眼
爆破工作
斜眼、直眼等掏槽方式
气腿式凿岩机炮眼深度1.6-2.5m,凿岩台车1.8-3m
三小:小直径钎杆、小直径炸药药卷、小直径钻头
正向装药和反向装药(效果较好)
连线方式:串并联,提高爆破效果
雷管采用毫秒延期电雷管,瓦斯煤尘不超过130ms,出水较大使用防水电雷管;爆破后进行通风和安全检查,通风排烟后班长和放炮员进入检查,工作面瞎炮处理、危石检查
装渣运输:出渣工作结束后,应快速钉道
装渣设备:铲斗后卸式、铲斗侧卸式、耙斗式(可平行作业)、蟹爪式、立爪式、新出产扒渣机
调车工作:耙矸机后铺设临时循环车场,调车器调车(浮动道岔调车器)
巷道支护
临时支护
一般都紧跟工作面,临时支护是永久支护的一部分
锚喷巷道临时支护,打设护顶锚杆只允许使用锚杆钻机,严禁使用风动凿岩机,拱线为准
金属支架临时支护,使用前探梁方式实现,长度4m,抵住山墙,在前探梁上放置顶梁并用背板背实
永久支护
锚喷支护:一掘一喷或两掘一喷以至三掘一喷
金属支架支护:底板松软要穿鞋,倾斜巷道设3-5度的迎山角
整体支护:现浇混凝土砌筑先墙后拱,最后封顶
岩石破碎、地压较大、大断面硐室,先锚喷支护,然后进行现浇混凝土支护的复合支护方式
综掘机施工
巷道与硐室的施工方法
巷道施工方法
一次成巷:掘进、永久支护、水沟掘砌视为整体,一次成巷
分次成巷:掘进和永久支护两个分部工程完成
硐室的施工方法
全断面施工法:稳定及整体性好的岩层,一般不超过4-5m,维护较难
分层施工法
正台阶施工:施工时形成台阶状,上工作面超前施工称为正台阶(每分层1.8-3m为宜或以起拱线作为上分层,上分层超前距离2-3m);如采用砌碹支护,上分层锚喷支护,砌碹工作落后于下分层掘进1.5-3m,距离太大,上分层出矸困难,距离太小,上分层钻眼困难
导硐施工法:地质条件复杂或断面特大硐室,可先掘进1-2个小断面巷道,然后刷帮、挑顶或卧底。一般反向施工交叉点时采用导硐施工法
巷道施工机械设备配套方案
方案
1、多台气腿式凿岩机钻眼—铲斗后卸式或耙斗式装载机装岩—错车场或道岔或调车器—矿车及电机车运输
2、多台气腿式凿岩机钻眼—铲斗后卸式或耙斗式装载机装岩—胶带运输机转载—矿车及电机车运输
3、多台气腿式凿岩机钻眼—铲斗后卸式或耙斗式装载机装岩—胶带运输机转载—立式矸石仓—矿车及电机车运输(金属矿常用)
4、多台气腿式凿岩机钻眼—铲斗后卸式或耙斗式装载机装岩—胶带运输机转载—水平矸石仓—矿车及电机车运输
5、凿岩台车钻眼—铲斗后卸式或耙斗式装载机装岩—胶带运输机转载—矿车及电机车运输
6、钻装机钻眼与装岩—胶带运输机转载—矿车及电机车运输
7、岩巷掘进机综合机械化作业线
巷道掘砌循环图标编制方法
正规循环作业
基本工序:工作面定向、炮眼布置、钻眼工作、装药联线、放炮通风、安全检查、洒水、临时支护、装岩与运输、清底、永久支护、水沟掘砌和管线安设
循环图标编制(10%的备用时间):总时间=交接班时间+不平行系数*装岩工作(60*面积*炸多深的矸石/装岩机生产率)+钻眼工作时间(炮眼数目*深度/钻机数量*钻速)+装药、连线时间+放炮通风时间
巷道施工通风防尘及降温方法
巷道施工通风
通风方式
压入:新鲜处10m以上,距工作面不大于10m,柔性风筒)
抽出:排风口风流方向下方,不得小于10m,有瓦斯涌出的不宜采用,刚性风筒或刚性骨架柔性风筒
混合(最佳):联合运用,压风吸风口与抽出抽入口距离不小于15m
通风设备:单机或双机同时使用
综合防尘:二氧化硅矽肺病,湿钻眼、湿喷浆;二高二隔一监控(高压喷雾降尘、高分子抑尘,隔尘水幕、隔离式呼吸器,工作面防尘监控)
巷道施工降温:采掘工作面超过30度、机电硐室超过34度,必须降温;四六工作制,保障睡眠时间
缓坡斜井施工方法及其应用
施工方法
全断面一次施工:边掘边锚,前掘后喷,小班单循环
台阶法施工
掘进机施工
斜井及倾斜巷道施工特点
斜井井筒施工方法
表土明挖段施工:边坡稳定,先墙后拱,边坡稳定性差,先拱后墙法,混凝土设计强度70%以上可回填
斜井表土暗挖段施工
干的多孔性表土,风镐挖掘
含水可用爆破法施工,孔深2m内,表土不稳定,导硐法、管棚法、金属棚背板法、锚喷网法作临时支护施工;含水较大,降低水位法、冻结法、帷幕、超前注浆、局部硬化
斜井从明槽进入暗挖的1-3m,明槽部分永久支护同时施工,稳定表土无水,可锚喷网支护
斜井基岩段施工:钻眼爆破发、掘进机法
斜井基岩段掘进方法:松软岩层,机械挖掘(小型短臂无尾挖掘机);钻爆法掘进,底部炮眼倾斜角度应适当大于斜井倾角,以防底板欠挖
斜井施工排矸和运输
装岩设备耙斗装岩机、挖掘机、装载机;斜井大于8度,轨道运输,矿车或箕斗;运矸双轨双套提升
一坡三挡(防跑车):斜井上口入口前,变坡点下方略大于一列车长度的地点,装车点上方,需设置挡车栏
斜井施工永久支护:锚喷支护方式,湿式混凝土喷射机
斜井施工排水:三级排水 工作面(一级);二级排水站(工作面后面适当位置,一开一备,10%的富余量);三级排水站(移动次数不宜过多)
斜井施工通风
独头施工:压风通风2000m,2*30kw,直径不小于800mm;3000m,2*55kw,直径1000mm;3000m以上,增加回风措施立井
双斜井:前期独立,后期施工联络巷,一个进一个回
倾斜巷道施工安全:防跑车装置并定期检查更换钢丝绳,每40m设置躲避硐并设红灯,红灯和语音提示装置